La première pile biologique, respectueuse de l’environnement, capable de produire de l’énergie à partir de substrats biodégradables en continue voit le jour. Cette réalisation développée par des chercheurs du Département de chimie moléculaire (CNRS/Université Grenoble Alpes) et du Centre de recherches sur les macromolécules végétales (CNRS) constitue un changement de paradigme dans le domaine des piles à base d’enzymes. Une preuve de concept qui ouvre de nouvelles perspectives pour le développement de biopiles implantables dans le corps humain. Ces travaux sont publiés dans la revue ACS Energy Letters.
Certaines piles biologiques – ou biopiles – convertissent l’énergie chimique en énergie électrique grâce à l’action catalytique d’enzymes. Leur utilisation est également envisagée in vivo, mais pour cela, les biopiles enzymatiques doivent produire de l’électricité de façon continue à long terme.
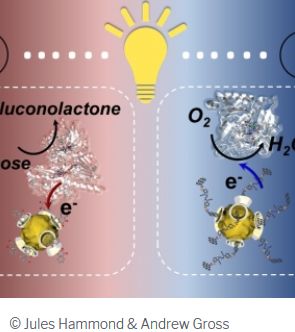
C’est ce qu’ont réussi pour la première fois des chercheurs du Département de chimie moléculaire (Equipe S. Cosnier, CNRS/Université Grenoble Alpes) et du Centre de recherches sur les macromolécules végétales (Equipe R. Borsali, CNRS). Pour cette avancée majeure, la biopile est basée sur une solution dans laquelle des transferts d’électrons s’effectuent entre l’enzyme et les électrodes de la pile par l’intermédiaire de molécules appelées médiateurs rédox. La pile consiste en deux électrodes insérées chacune dans un compartiment perméable permettant la libre circulation du substrat (glucose à l’anode et oxygène à la cathode) tout en emprisonnant les enzymes et les médiateurs rédox autour des électrodes. Une difficulté technique était d’empêcher les médiateurs rédox de taille équivalente à celle du glucose, de franchir la paroi perméable englobant l’électrode. Les chercheurs les ont alors piégés à la périphérie et à l’intérieur de « glyconanoparticules » obtenues par auto-assemblage de copolymères d’origine naturelle à base de cyclodextrine. Ces nanoparticules de taille modulable (20-400 nm), sont aisément fonctionnalisables par une variété de médiateurs rédox via des réactions d’inclusion avec les motifs cyclodextrines.